La détection précoce de la maladie d’Alzheimer, et de ses complications, est un problème médical majeur chez les adultes porteurs de trisomie 21. La Fondation Jérôme Lejeune soutient la recherche de biomarqueurs d’Alzheimer pour améliorer le diagnostic de cette maladie et, par conséquent, sa prise en charge chez les personnes atteintes de trisomie 21.
Les personnes atteintes de trisomie 21 ont un risque accru de développer une maladie d’Alzheimer (MA). Les scientifiques pensent que ce risque accru est en partie dû à la présence du gène APP sur le chromosome 21. Celui-ci contient la protéine précurseur de l’amyloïde impliquée dans les modifications du cerveau associées à l’Alzheimer.
Des études ont montré qu’à l’âge de 40 ans, les cerveaux de l’immense majorité des individus porteurs de trisomie 21 présentent des niveaux significatifs de plaques amyloïdes et d’enchevêtrements neurofibrillaires « tau* ». Dépôts anormaux de protéines, ils sont considérés comme caractéristiques de la maladie d’Alzheimer, et interfèrent avec la fonction des cellules neuronales et la communication entre les cellules du cerveau. Malgré la présence de ces modifications cérébrales, toutes les personnes atteintes de trisomie 21 ne développent pas systématiquement de maladie d’Alzheimer. Pourtant, la prévalence augmente avec l’âge des patients et atteint 80 % après 65 ans.
Diagnostic de la maladie d’Alzheimer associée à la trisomie 21
Ce diagnostic reste difficile, car les symptômes peuvent passer inaperçus en raison de la déficience intellectuelle chez l’adulte porteur de trisomie 21, cette déficience rendant difficile l’évaluation des modifications des fonctions cognitives. En outre, les premiers symptômes peuvent être masqués par des comorbidités médicales susceptibles d’affecter la cognition, telles que l’apnée du sommeil, les troubles neurosensoriels, l’hypothyroïdie et la dépression. Le diagnostic clinique se fait avec les mêmes critères que ceux utilisés dans la population générale. L’évaluation neuropsychologique est en cours de standardisation, avec l’aide du consortium européen Horizon 21, soutenu par la Fondation et dont l’Institut Jérôme Lejeune est un des membres très actif. Les fonctions cognitives et leur déclin doivent être évalués à l’aide de tests neuro-psychologiques adaptés, et accompagnés parfois de neuro-imagerie et de biomarqueurs dosés dans le liquide céphalorachidien et/ou dans le sang. Ces analyses nécessitent la coopération de chaque patient et doivent être réalisées dans des centres spécialisés, comme l’Institut Jérôme Lejeune.
Biomarqueurs du LCR et du sang (voir le schéma ci-contre)
Plusieurs biomarqueurs basés sur les fluides biologiques ont été développés pour devenir des tests diagnostiques de la MA.
Le liquide céphalo-rachidien (LCR) prélevé par ponction au niveau du rachis : les biomarqueurs du LCR ont une excellente performance diagnostique. Ils sont intégrés dans les critères de diagnostic de la recherche pour la MA sporadique, chez l’adulte non trisomique, et couramment utilisés dans les essais cliniques. Ces biomarqueurs peuvent être utilisés en pratique clinique chez l’adulte porteur de trisomie 21, pour étayer un diagnostic de troubles cognitifs légers, ou de démence due à la MA. La recherche se poursuit sur d’autres marqueurs prometteurs dans le LCR.
Des tests sanguins : les récentes avancées technologiques ont permis d’identifier les mêmes biomarqueurs dans des échantillons de sang ordinaires, ce qui est avantageux compte tenu de la facilité avec laquelle on peut les collecter. La concentration de biomarqueurs dans le sang, y compris les marqueurs de dépôts anormaux de protéines et de neurodégénérescence, sont bien corrélés avec les concentrations trouvées dans le LCR.
Biomarqueurs de neuro-imagerie :
Les techniques de neuro-imagerie sont largement utilisées pour étudier la structure et la fonction du système nerveux. Chaque technique présente ses limites, ce qui a conduit au développement de la neuro-imagerie multimodale, qui combine les données obtenues provenant de chaque technique. La recherche analyse la neuro-imagerie multimodale chez les adultes atteints de trisomie 21 en combinant le PET scan et l’IRM.
La Tomographie par émission de positons (PET scan) est utilisée pour mesurer la concentration de molécules dans le cerveau, à l’aide de traceurs radioactifs spécifiques. Dans le cas de la MA, la protéine β-amyloïde, la protéine tau, le métabolisme du glucose et l’activation de la microglie, entre autres, peuvent être étudiés. La présence d’une modification de ces éléments plaide en faveur d’un diagnostic positif de la maladie d’Alzheimer.
L’Imagerie par résonance magnétique (IRM) est utilisée pour créer des images détaillées du cerveau à l’aide d’un champ magnétique, et d’ondes radio générées par ordinateur. Il est souvent réalisé en même temps qu’un PET scan pour obtenir des informations détaillées sur la forme et la structure du cerveau des patients. Aux stades avancés de la maladie, des signes de neurodégénérescence sont souvent observés (atrophie).
Recherches financées par la Fondation Jérôme Lejeune
Le projet de l’équipe du Dr. Beatriz Sánchez Moreno en Espagne, visant à améliorer le diagnostic clinique de la MA chez les personnes atteintes de trisomie 21, a été sélectionné lors du dernier appel à projets de la Fondation Jérôme Lejeune. Il démontre l’utilité d’une analyse semi-automatique de la tomographie cérébrale assistée par ordinateur (CT scan) comme technique accessible, déjà évaluée dans la population générale. L’équipe va étudier l’atrophie cérébrale en fonction de l’âge et du déclin cognitif dans une cohorte de personnes atteintes de trisomie 21, et corréler ces mesures avec les biomarqueurs plasmatiques de la MA, afin de trouver un modèle simple qui pourrait aider à prédire le déclin cognitif.
* Protéine associée impliquée dans des maladies neurodégénératives telles que la maladie d’Alzheimer.
De plus, avec l’aide de la Fondation, l’Institut Jérôme Lejeune participe en tant que centre investigateur à plusieurs études.
L’étude SHATAU7-IMATAU, en collaboration avec l’hôpital Sainte-Anne à Paris, le Commissariat à l’Énergie Atomique et aux Énergies Alternatives et le CRB-BioJeL. Cette étude a pour but d’analyser si l’imagerie PET-tau (Tomographie par Emission de Positons en utilisant un marqueur radioactif de la protéine Tau) permet de détecter un dépôt protéique tau à un stade préclinique de la maladie d’Alzheimer. La comparaison est établie avec une atrophie corticale mesurée dans une population d’adultes porteurs de trisomie 21 indemnes cliniquement de maladie d’Alzheimer.
L’étude TriAL 21, en collaboration avec l’hôpital Lariboisière, le groupe Hospitalier Paris Saint-Joseph, l’hôpital Pitié-Salpêtrière et CRB-BioJeL. Cette étude a pour objectif principal d’identifier des facteurs prédictifs influençant l’âge d’apparition de la maladie d’Alzheimer chez des patients adultes porteurs de trisomie 21. L’étude permettra également de suivre les fonctions cognitives (mémoire, langage, raisonnement), d’identifier des biomarqueurs et d’évaluer la tolérance des patients à ces examens.
Horizon 21 : projet collaboratif auquel participent 10 centres spécialisés européens dont l’Institut Jérôme Lejeune. Cette étude vise à préparer un essai thérapeutique pour la maladie d’Alzheimer dans la population porteuse de trisomie 21. Leur premier objectif est d’harmoniser les protocoles diagnostiques entre les différents pays et d’obtenir une échelle d’évaluation unique pour les études cliniques et le suivi des patients. Les chercheurs souhaitent également définir des marqueurs de progression de la maladie, et identifier des marqueurs génétiques de risque ou protecteurs, dès la phase pré-symptomatique de la maladie.
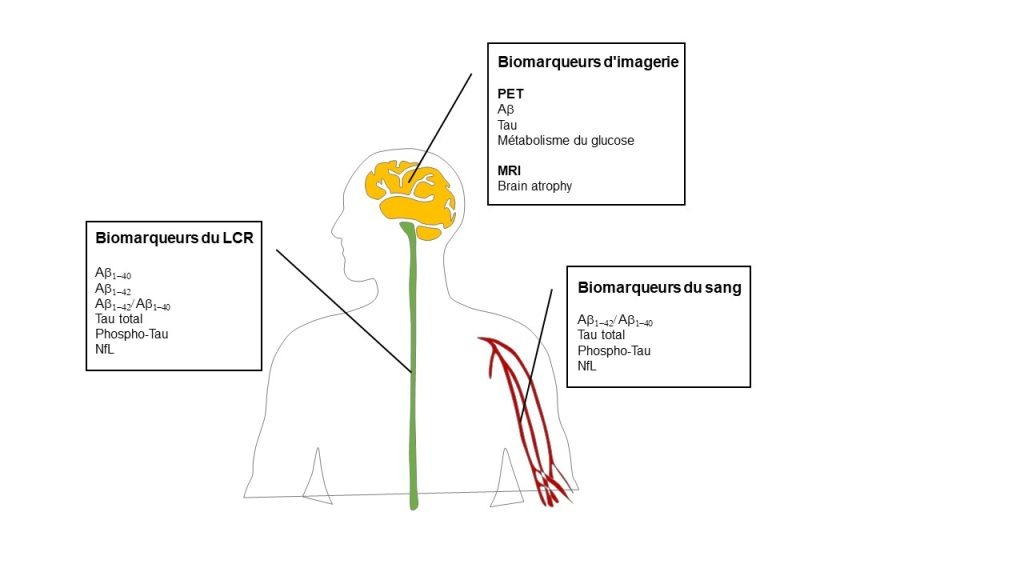
Biomarqueurs pouvant être utilisés pour détecter des modifications dans le cerveau qui pourraient aider à diagnostiquer la maladie d’Alzheimer chez les personnes porteuses d’une trisomie 21.
Abbréviations :
Aβ : bêta-amyloïde
Aβ1-40 : peptide amyloïde de 40 aminoacides
Aβ1-42 : peptide amyloïde de 42 aminoacides
Aβ1-42/Aβ1-40 : ratio peptide bêta-amyloïde 42/40.
Phospho-Tau : Tau phosphorylée
NfL : neurofilament à chaine légère
- Catégories
Derniers articles
Recevez chaque mois les expertises et les événements de la fondation dans votre boite email !
« * » indique les champs nécessaires